Een eiwit bestaat uit aminozuren en heeft een ruimtelijke structuur.
De ruimtelijke structuur heeft een ‘sleutel-slot’ principe met zijn substraat. Het substraat is de stof waaraan een enzym zich hecht.
Na hechting van een enzym aan zijn substraat, vindt er over het algemeen een verandering van het substraat plaats.
Door dit sleutel slot principe is een enzym substraat specifiek ofwel hij past maar op één substraat.
De actie van een enzym is ook veelal beperkt tot één reactie.
Een enzym is dus ook reactie specifiek. Veel enzymen bestaan niet alleen uit een eiwitdeel, maar ook nog uit een tweede, niet eiwitdeel. Dit niet eiwitdeel heet een co enzym.
Een co-enzym is kan een vitamine zijn of wordt van een vitamine gemaakt zoals van vitamine C en K.
Het hulpje van het enzym kan ook een anorganische stof zijn en wordt dan cofactor genoemd.
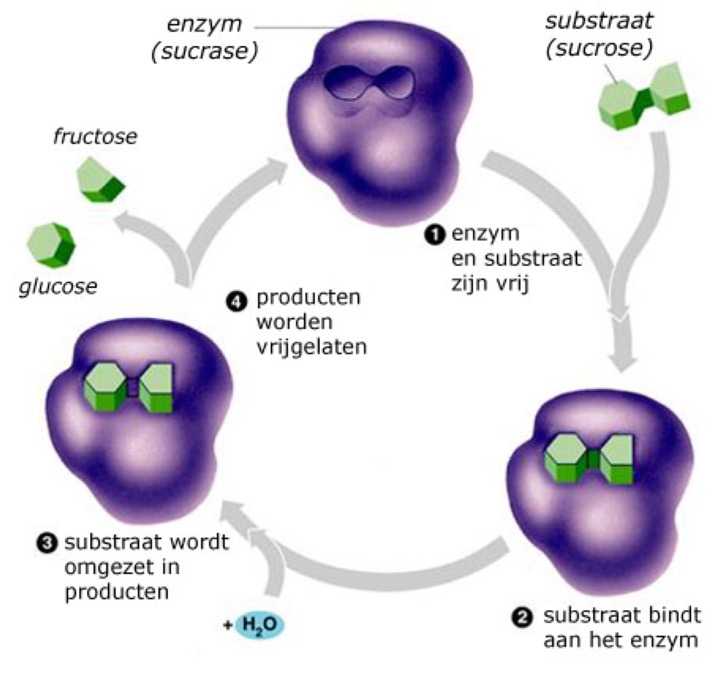
Enzymoptimum
De werking van een enzym kan beïnvloed worden door verschillende omstandigheden:
De temperatuur en de zuurgraad hebben invloed op de structuur en kan ervoor zorgen dat het substraat niet meer past of zelfs dat de hele structuur van het eiwit verloren gaat.
De activiteit van een enzymoplossing is weer te geven in een diagram.
Zo’ n diagram geeft aan hoe effectief de enzymoplossing is, maar niet hoe effectief elk enzymmolecuul afzonderlijk is. Zo kunnen de enzymmoleculen per stuk minder geschikt zijn om een substraat te binden maar door de snelheid van de moleculen toch veel omzettingen verrichten.
Het punt waarop een enzymoplossing het beste werkt heet het enzymoptimum.
Een vergelijking: hard werken (hoge temperatuur) met een botte bijl (minder goede enzymstructuur) kan meer opleveren dan minder hard werken (lagere temperatuur) met een scherpe bijl (betere enzymstructuur). De mindere enzymstructuur ten gevolge van temperatuurverhoging heet denaturatie door temperatuur. Boven een bepaalde temperatuur is denaturatie niet meer te herstellen.
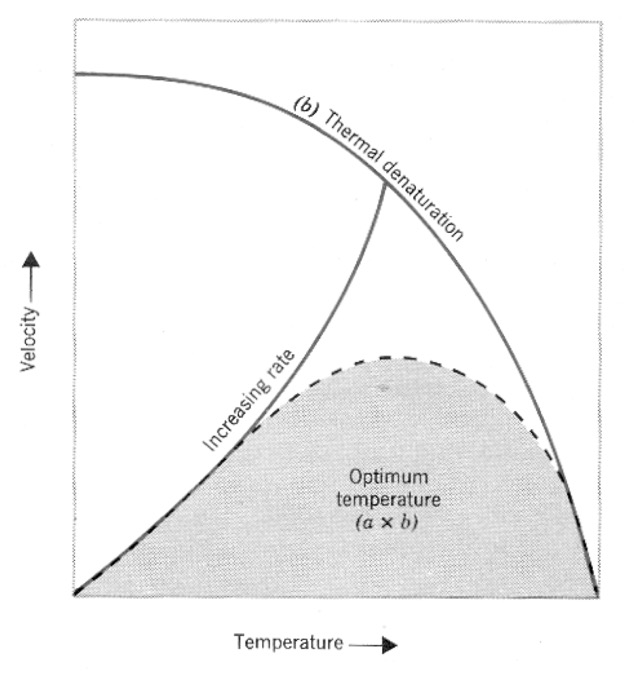
De snelheid van zowel enzymmoleculen als substraatmoleculen neemt toe en daarmee de reactiesnelheid. De structuur van een enzym wordt echter steeds minder geschikt voor het binden van het substraat: Denaturatie. Er is een punt waarop de enzymoplossing het beste werkt: de optimumtemperatuur. Dat is echter niet de temperatuur voor optimale structuur van het enzym.
Enzymremming en stimulering
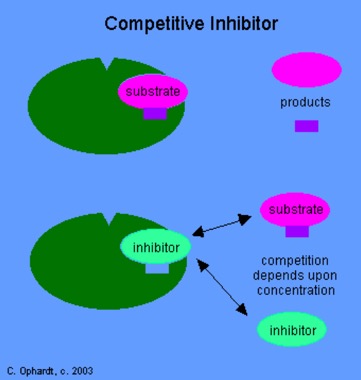
Een andere stof kan de plaats innemen van het substraat waardoor een groot deel van de enzymmoleculen is bezet, afhankelijk van de concentratie van de concurrent. Dit heet een competitieve remmer ofwel competitieve inhibitor.
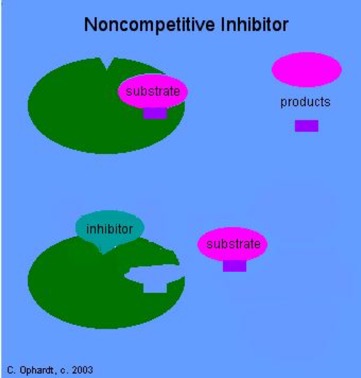
Een stof kan zich binden aan een enzym en daarmee de enzymstructuur zo veranderen, dat het substraat niet meer past. Dat heet een niet competitieve remmer ofwel niet competitieve inhibitor.
Hulpstof
Een stof kan een enzym juist zo veranderen, dat er een substraat in juist wel in past.
Dat kan gebeuren door de werking van een ander enzym of door de binding van een andere stof. In dat laatste geval is er sprake van een cofactor. De cofactor kan organisch zijn: een co enzym of anorganisch, bijvoorbeeld een metaal ion activator. De inactieve vorm heet een pro-enzym ofwel zymogeen. Een voorbeeld van een inactief enzym dat actief gemaakt worden door een ander enzym is het bloedstollingseiwit fibrinogeen dat door trombine in fibrine kan veranderen. Pepsinogeen in het maagsap is een eiwit verterend enzym dat pas actief wordt als er zoutzuur (cofactor) bijkomt. Pepsinogeen heet in deze actieve vorm pepsine. De cofactor treedt dus op als activator. Pepsinogeen kan op die manier geen lichaamseigen eiwit omzetten in de cel waar het geproduceerd wordt.